El Modelo de Pez Cebra en las Fases Tempranas del Descubrimiento y Registro de Fármacos
El proceso de descubrimiento y desarrollo de fármacos es largo y costoso, con una duración promedio de 10 a 15 años y una inversión de aproximadamente 2,6 billones de dólares. Menos del 12% de los candidatos que llegan a ensayos clínicos de fase I son finalmente aprobados por la FDA.
Un porcentaje significativo de compuestos se excluyen debido a problemas de seguridad en las primeras etapas del proceso de investigación y desarrollo (I+D)?. Para optimizar este proceso, es crucial implementar cribados de toxicidad efectivos que puedan identificar los mejores candidatos desde el inicio, minimizando pérdidas económicas y de tiempo. Entre los métodos innovadores utilizados, el modelo de pez cebra (Danio rerio) ha demostrado ser un nuevo modelo alternativo (NAM) eficaz y rentable para los estudios de cribado de toxicidad en las primeras etapas del descubrimiento de fármacos??.
Ventajas del modelo de pez cebra en I+D
El pez cebra ha ganado popularidad en la investigación farmacéutica por sus múltiples ventajas genéticas, físicas y económicas. Este modelo in vivo alternativo combina diversas características que lo hacen ideal para estudios preclínicos:
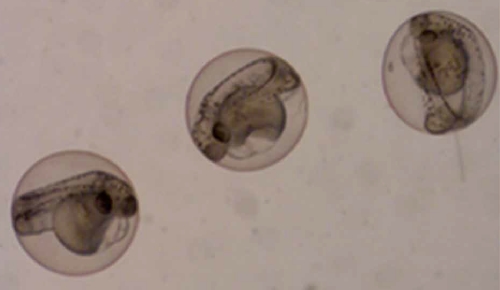
- Rentabilidad y Mantenimiento: El pez cebra es un modelo rentable y accesible de mantener. Su pequeño tamaño y transparencia en estado de larva son ideales para la observación y el análisis en investigaciones.
- Alta Productividad y Rápido Desarrollo: Una pareja de pez cebra puede producir entre 100 y 300 huevos por semana, con un desarrollo rápido que permite obtener resultados en poco tiempo.
- Similitudes Genéticas y Anatómicas con Humanos: Como vertebrado, el pez cebra comparte una alta homología genética con los humanos (más del 70%) y comparte alrededor de 80% de los genes implicados en enfermedades. Además, tiene grandes similitudes anatómicas en órganos como el corazón, cerebro, páncreas, riñones e hígado.
- Relevancia Biológica y Rapidez en los Ensayos: Permite realizar estudios con organismos completos de manera rápida y coste efectiva, lo que es crucial para la investigación farmacéutica en etapas tempranas??.
Biobide
Biobide -Grupo BIAT (ticker BST)- es una Organización de Investigación por Contrato (CRO) especializada en el modelo alternativo de pez cebra que lleva más de 19 años ofreciendo y desarrollando estudios de toxicidad y eficacia personalizados a empresas farmacéuticas, biotecnológicas, químicas, cosméticas y nutracéuticas, bajo un entorno de Buenas Prácticas de Laboratorio (BPL) como estándar de calidad.
Para acelerar el proceso de desarrollo de fármacos, los investigadores pueden utilizar diferentes ensayos para determinar la toxicidad o la eficacia de los candidatos. Existen diferentes tipos de ensayos según el propósito. Los ensayos de eficacia ayudan a validar si la actividad de un candidato puede fundamentarse, mientras que los ensayos de toxicidad ayudan a determinar la presencia de sustancias tóxicas dentro de un fármaco, pudiendo ser generales o específicos para determinados órganos. Los ensayos de ecotoxicidad, por su parte, ayudan a determinar la presencia de sustancias potencialmente peligrosas en el ecosistema.
A continuación, se describen los ensayos más comunes y de mayores prestaciones llevados a cabo en el modelo de pez cebra para las etapas de descubrimiento de fármacos y de registro de productos.
Ensayos de toxicidad general
Ensayo Acutetox
La toxicidad aguda es un término general para cualquier efecto nocivo causado por una única exposición a una sustancia tóxica. Los efectos suelen manifestarse casi inmediatamente después de la exposición, aunque puede haber un período de latencia.
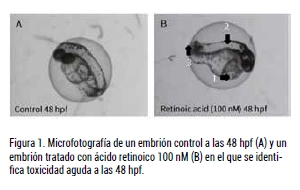
Siguiendo las directrices de la OECD (Organización para la Cooperación y el Desarrollo Económico), específicamente la TG 236 del Ensayo de toxicidad aguda en embriones de peces (FET), Biobide ha puesto a punto un ensayo simplificado, llamado Acutetox de toxicidad aguda en pez cebra eficiente, rápido y coste efectivo con el fin de priorizar compuestos de grandes bibliotecas. Los embriones en estadio de 2-4 horas post-fertilización (hpf) se incuban con 8 concentraciones del compuesto utilizando ácido retinoico como control positivo.
Durante 96 horas de tratamiento se monitorizan los embriones y se mide la inducción de toxicidad como presencia de cualquiera de los 4 parámetros principales descritos por la Guía FET (coagulación, latido del corazón, formación de somitas y desprendimiento de la cola). Posteriormente se obtienen imágenes de efectos significativos y una curva de concentración-efecto.
A continuación, se muestra una microfotografía en la que se compara una muestra de embrión control a 48 hpf (A) y un embrión tratado con ácido retinoico 100 nM (B) en el que se identifica toxicidad aguda a las 48 hpf con signos claros como defectos en el corazón (1), falta de somitas (2) y defectos en la cola (3).
Los estudios de toxicidad aguda en pez cebra son una buena herramienta para evaluar la toxicidad aguda de candidatos a fármacos en la fase preclínica temprana. Por otra parte, el ensayo Acutetox es un ensayo eficiente en tiempo y rentabilidad, en comparación con otros ensayos utilizados actualmente.

Ensayo Teratotox
Este ensayo permite evaluar el potencial de un fármaco para interferir en el desarrollo normal y causar efectos adversos en la descendencia. La toxicidad reproductiva es una de las principales preocupaciones y diferentes directrices, como la ICH S5(R2), establecen la necesidad de evaluar la seguridad química durante el proceso de desarrollo de un fármaco o antes de su comercialización.
El pez cebra es un modelo in vivo adecuado para los estudios teratogénicos ya que sus embriones se fertilizan externamente y se desarrollan rápidamente, de forma que los resultados pueden analizarse desde las 2 - 4 horas después de la fertilización hasta sus 5 días, durante el desarrollo de los órganos.
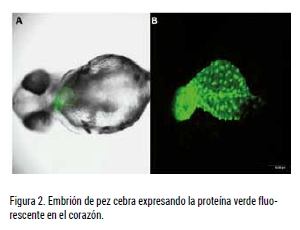
Para este ensayo se podría utilizar una línea de embriones de pez cebra que expresan una proteína verde fluorescente en el corazón, tal y como se muestra en la siguiente imagen:
A las 2-4 hpf los embriones se tratan a 8 concentraciones por compuesto y se incuban hasta los 2 y 4 días post-fertilización (dpf), cuando son analizados bajo el estereoscopio. De esta forma se calcula la concentración mínima a la que se induce la letalidad y se analizan diferentes órganos y procesos, incluidos puntos finales teratogénicos y tóxicos. Se calculan así los valores de EC50, LC50 para el Índice Teratogénico (TI) y NOAEL. También pueden llevarse a cabo análisis complementarios como la biodisponibilidad por HPLC-MS/MS, la histopatología o expresión de genes de interés.
Ensayos de toxicidad específica
Ensayo de Neurotoxicidad
Diferentes estudios han detectado estrechas similitudes en las vías de señalización neuronal y las regiones funcionales del cerebro entre los humanos y el pez cebra. Se han observado alteraciones en el patrón de movilidad de las larvas inducidas por fármacos conocidos que apoyan firmemente al pez cebra como modelo predictivo de la neuroactividad en humanos. Biobide ha desarrollado un ensayo para evaluar la neurotoxicidad basado en las alteraciones del comportamiento en las respuestas a los cambios de luz-oscuridad.
Para este ensayo se utilizan embriones de pez cebra de 5 dpf y se tratan durante 2 horas con 5 concentraciones por compuesto. La actividad locomotora/respuesta fotomotora del pez cebra se analiza durante 40 minutos alternando fotoperiodos de 10 minutos utilizando el sistema DanioVision alimentado por Ethovision (Noldus). Además, también se pueden analizar factores como la viabilidad, la formación de la vejiga natatoria, la presencia de edema, defectos en la forma del cuerpo y la pérdida del equilibrio. Se pueden analizar más de 10 parámetros en base a la distancia recorrida, la velocidad, duración del movimiento y la frecuencia.
El efecto neurotóxico también puede analizarse durante el desarrollo, con el ensayo de Desarrollo de Neurotoxicidad (DNT), exponiendo los embriones a 5 concentraciones de los compuestos de interés desde las 3-6 hpf hasta las 120 hpf, durante todo el desarrollo, e incluyendo no solo el análisis del movimiento sino también las alteraciones morfológicas de los mismos.
Ensayos de ecotoxicidad
El campo de la ecotoxicología ha avanzado rápidamente en los últimos 50 años y se refiere al estudio de los efectos que las sustancias químicas y otros contaminantes tienen no solo sobre la salud humana sino en el medio ambiente. Muchas sustancias creadas por el hombre, como los pesticidas y los productos químicos, contienen componentes que pueden interactuar con los organismos del medio ambiente, dañando el ecosistema del planeta y provocando contaminación ambiental. También existen toxinas en compuestos naturales, como el plomo y el arsénico, que pueden ser muy peligrosos para la salud humana. Para evaluar la seguridad y/o los efectos nocivos de estos productos químicos, existen varias pruebas de ecotoxicidad. Estos métodos evalúan el efecto de la supervivencia, reproducción, crecimiento y rendimiento después de la exposición a sustancias químicas.
Biobide ha desarrollado diferentes ensayos de ecotoxicidad miniaturizados basados en las guías de la OECD pero de forma simplificada, incluida la prueba de toxicidad de algas en microplacas basándose en la guía de la OECD 201, el ensayo de inmovilización de Daphnia magna tomando como referencia la guía OCDE 202, el ensayo de toxicidad aguda en embrión de pez cebra (FET) (OECD 236) o el ensayo de disrupción endocrina, como fases de screening primario, y además puede realizar los ensayos en su forma no miniaturizada, siguiendo las guías y bajo BPLs. Entre ellos destaca el ensayo de disrupción endocrina que se describe en mayor detalle a continuación.
Ensayo de disrupción endocrina
Los compuestos que son disruptores endocrinos están muy extendidos en el medio ambiente y existe una creciente preocupación por los impactos ambientales que pueden generar ya que tienen la capacidad de alterar el sistema endocrino y pueden provocar efectos adversos en el desarrollo, la reproducción, la función neurológica y/o inmune tanto en los seres humanos, como en la vida silvestre. Esta preocupación ha aumentado debido al papel fundamental que desempeñan las hormonas tiroideas durante el desarrollo.
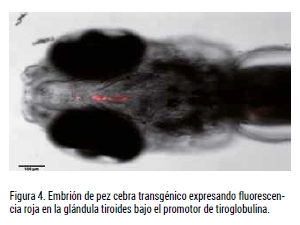
Biobide ha desarrollado, validado y publicado un ensayo en pez cebra para detectar compuestos que tienen acción de disruptores tiroideos (TD) utilizando embriones transgénicos tg(tg:mcherry), que expresan fluorescencia roja en la glándula tiroides bajo el promotor de tiroglobulina.
Los aumentos en los niveles de tiroglobulina generan un aumento de la fluorescencia por medio de análisis de imágenes y de esta forma, la intensidad de la señal se puede evaluar in vivo para detectar y caracterizar el potencial para alterar el tiroides, ya sea directamente o después de la metabolización.
Este ensayo se compone de una primera etapa para determinar la concentración máxima tolerada (MTC), de forma que se determinen los parámetros LC50, EC50 y EC10. Para ello, los embriones de pez cebra de 48 hpf se exponen a 8 concentraciones de los compuestos de interés y a las 120 hpf se analizan los efectos sistémicos y del desarrollo.
Posteriormente, se lleva a cabo el ensayo de disrupción tiroidea basado en fluorescencia, en el que los embriones de pez cebra expresando la proteína fluorescente mcherry en la glándula tiroidea se exponen a 5 concentraciones de los compuestos de interés. Los embriones se exponen y a las 120 hpf se analizan bajo un microscopio de fluorescencia por medio de imágenes. Los datos son analizados y se determina el Benchmark Concentration (BMC) y el Índice de disrupción tiroidea (TDI). Finalmente, el estudio puede completarse con un análisis de expresión de genes como tshβ, tg y tpo para obtener una caracterización más amplia del efecto disruptor del tiroides.
Conclusión
El pez cebra se ha consolidado como un modelo alternativo (NAM) esencial en las fases tempranas del descubrimiento y desarrollo de fármacos. Su relevancia biológica, rentabilidad, y eficiencia lo convierten en una herramienta invaluable para la investigación preclínica. Al proporcionar datos precisos y rápidos sobre la toxicidad y la eficacia de los compuestos, el pez cebra ayuda a acelerar el proceso de descubrimiento de fármacos, mitigando los costes y mejorando la tasa de éxito de los candidatos que avanzan a ensayos clínicos.
Referencias
- OECD (2021), Test No. 250: EASZY assay - Detection of Endocrine Active Substances, acting through estrogen receptors, using transgenic tg(cyp19a1b:GFP) Zebrafish embrYos, OECD Guidelines for the Testing of Chemicals, Section 2, OECD Publishing, Paris, https://doi.org/10.1787/0a39b48b-en.
- OECD (2013), Test No. 236: Fish Embryo Acute Toxicity (FET) Test, OECD Guidelines for the Testing of Chemicals, Section 2, OECD Publishing, Paris, https://doi.org/10.1787/9789264203709-en.
- OECD (2011), Test No. 201: Freshwater Alga and Cyanobacteria, Growth Inhibition Test, OECD Guidelines for the Testing of Chemicals, Section 2, OECD Publishing, Paris, https://doi.org/10.1787/9789264069923-en.
- OECD (2004), Test No. 202: Daphnia sp. Acute Immobilisation Test, OECD Guidelines for the Testing of Chemicals, Section 2, OECD Publishing, Paris, https://doi.org/10.1787/9789264069947-en.
- Jaka, O., Iturria, I., Martí, C., Hurtado de Mendoza, J., Mazón-Moya, M., Rummel, C., AMJ, W., & Muriana, A. (2023). Screening for chemicals with thyroid hormone-disrupting effects using zebrafish embryo. Reproductive Toxicology (Elmsford, N.Y.), 121, 108463–108463. https://doi.org/10.1016/j.reprotox.2023.108463
- Hamm, J. T., Hsieh, J.-H., Roberts, G. K., Collins, B., Gorospe, J., Sparrow, B., Walker, N. J., Truong, L., Tanguay, R. L., Dyballa, S., Miñana, R., Schiavone, V., Terriente, J., Weiner, A., Muriana, A., Quevedo, C., & Ryan, K. R. (2024). Interlaboratory Study on Zebrafish in Toxicology: Systematic Evaluation of the Application of Zebrafish in Toxicology’s (SEAZIT’s) Evaluation of Developmental Toxicity. Toxics (Basel), 12(1), 93-. https://doi.org/10.3390/toxics12010093.
| Nombre | |
|---|---|
| Empresa | Biat Group |
| Cargo |
Si continúas navegando, aceptas su uso.
Más información
Política de privacidad | Cookies | Aviso legal | Información adicional| miembros de CEDRO










































