Ensayos Clínicos con Productos Sanitarios en España: Un Análisis Integral
El sector de los productos sanitarios (PS) está experimentando un gran crecimiento en España en los últimos años. Este crecimiento se ve impulsado en parte por la revolución digital, con multitud de nuevos PS que integran software y la inteligencia artificial, permitiendo transformar la manera en que se diagnostican y tratan enfermedades.
En paralelo, los ensayos clínicos también están en auge. En este artículo nos centraremos en esta transformación, examinando el papel de España en la innovación de los productos sanitarios y la investigación clínica asociada, dentro del marco regulatorio europeo y las tendencias globales.

Ensayos clínicos con productos sanitarios
Los ensayos clínicos son fundamentales para proporcionar evidencia clínica sobre el funcionamiento y la seguridad de los PS, tanto para la validación de nuevos PS (ensayos pre-comercialización) como la vigilancia de aquellos que ya están en el mercado (ensayos post-comercialización). Estos ensayos propulsan el avance de la medicina, permitiendo la incorporación de la innovación a la práctica clínica y contribuyendo a la mejora de la calidad de vida y bienestar de los pacientes.
Ensayos clínicos en España
Posicionamiento en ensayos clínicos
A pesar de los desafíos, España se ha posicionado como uno de los líderes mundiales en investigación clínica, con un aumento progresivo del 5,7% año a año desde 2012 del número de inversiones y, por tanto, del número ensayos clínicos realizados. Según datos de la Organización Mundial de la Salud (OMS) de 2022, España es el décimo país a nivel mundial en cuanto a número de ensayos clínicos activos, con 2.092 ensayos clínicos activos en 2022 y el noveno en la última década. A nivel europeo, España es el cuarto país con mayor número de ensayos clínicos activos en 2022 y el que muestra mayor crecimiento en participación desde 1999 comparado con países como Alemania, Reino Unido, Francia, Países Bajos o Italia2. Estos datos incluyen todo tipo de ensayos, aunque predominan las investigaciones en fases tempranas del desarrollo. En 2023, el 61% de los ensayos clínicos fueron de fase I y II, mientras que un 36% fueron de fase III y un 3% de fase IV1. La mayoría de los ensayos clínicos en España están centrados en el tratamiento de cáncer (25% de los ensayos realizados en 2022), condiciones neuropsiquiátricas, patologías endocrinas e inmunológicas y enfermedades cardiovasculares2. Además, más de un 20% de los ensayos clínicos realizados en 2023 en España se centraron en el tratamiento y estudio de enfermedades raras.
Ensayos clínicos con medicamentos vs producto sanitario
Los ensayos clínicos en España distinguen claramente entre medicamentos de uso humano y productos sanitarios. Mientras que los ensayos clínicos con medicamentos suelen requerir pruebas más extensas y fases detalladas (I, II, III, IV) para demostrar su eficacia, los ensayos clínicos con producto sanitario se centran en demostrar la seguridad y el funcionamiento del producto en investigación.
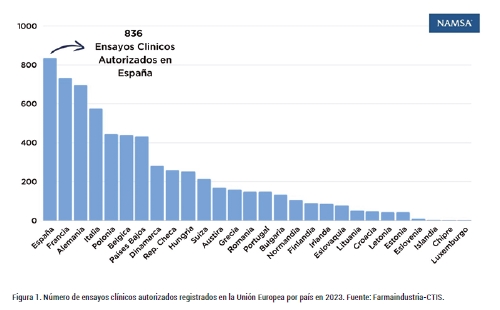
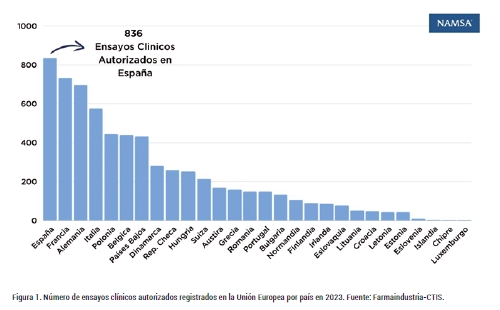
Si nos centramos en los ensayos clínicos con medicamentos, España sube al número uno del ranquin de la Unión Europea, participando en hasta el 43% de los ensayos clínicos activos con 836 ensayos clínicos registrados en el Registro Español de Estudios Clínicos (REEC) y la plataforma CTIS (Clinical Trials Information System), por encima de países como Francia (734), Alemania (697) o Italia (576), según datos de 2023.
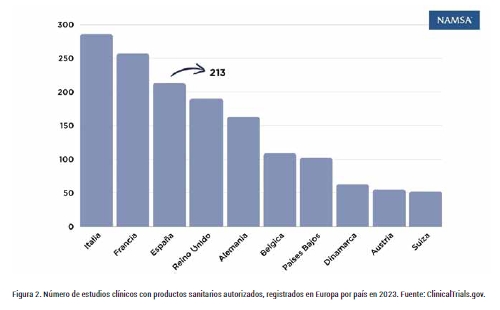
En cuanto a ensayos con productos sanitarios, según datos de 2023, España es el tercer país europeo con mayor participación en ensayos clínicos con producto sanitario, solamente por detrás de Italia y Francia, participando en el 43% de los estudios clínicos autorizados en Europa. Según datos del 2023, en España se registraron 213 estudios clínicos con productos sanitarios, de los cuales el 70% de fueron intervencionales.
Promoción de los ensayos clínicos
Si analizamos los datos de los promotores de ensayos clínicos en España, vemos claramente como la mayoría de los ensayos clínicos están promocionados por la industria farmacéutica y MedTech (aproximadamente sobre el 80% según datos de los últimos 10 años).
El 15-20% restante de ensayos realizados en España son iniciados por hospitales, centros públicos de investigación y otras instituciones, otorgándoseles el nombre de ensayos clínicos académicos. Cabe destacar, que la mayoría de los ensayos clínicos financiados por la industria están centrados en estudios oncológicos (45%), mientras que la mayoría de ensayos clínicos académicos se centran en enfermedades infecciosas, en patologías del SNC o cardiovasculares, con una menor proporción de ensayos oncológicos6. Las razones por las que el número de ensayos clínicos académicos es bajo en comparación con la industria se centran sobre todo en la falta de tiempo y recursos especializados:
- Falta de recursos económicos necesarios para desarrollar un ensayo clínico complejo, especialmente en fases tempranas.
- Falta de unidades de ensayos clínicos con conocimiento sobre el diseño y desarrollo de ensayos clínicos.
- Falta del personal capacitado requerido. El profesional sanitario o investigador suele realizar las actividades del ensayo clínico fuera del horario laboral.
- Las actividades de gestión y análisis de datos requieren tiempo y conocimientos profundos sobre ensayos clínicos.
Claves para la atracción de ensayos clínicos
Algunas de las claves de nuestro país que explican el crecimiento en el número de ensayos clínicos son:
1. Potencial de reclutamiento de pacientes: España cuenta con un gran potencial de reclutamiento debido a su demografía y a la prevalencia de enfermedades mentales, cardiovasculares, cerebrovasculares, pulmonares y cáncer (mama y colón), donde la inversión y el número en ensayos clínicos para el tratamiento de estas enfermedades es elevado.
2. Infraestructura y capacidades de investigación: En cuanto a la infraestructura y capacidades de investigación, España cuenta con uno de los mejores sistemas sanitarios de Europa, con una sólida red de hospitales de primer nivel, centros de investigación de alta calidad, una red de profesionales altamente cualificados y unidades especializadas en ensayos clínicos4. Estas características permiten a España llevar a cabo ensayos clínicos complejos y avanzados.
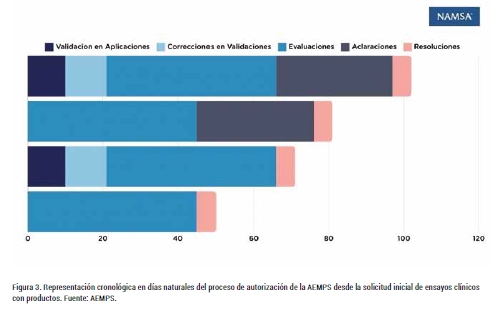
3. Procesos de aprobación regulatoria y ética: Los ensayos clínicos en España deben seguir procesos regulatorios y éticos estrictos, supervisados por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) y los Comités de Ética de la Investigación. Estos procesos garantizan la protección de los participantes y la integridad de los datos obtenidos. En España existe un proceso de aprobación regulatoria claramente definido y eficiente, lo que permite conseguir la aprobación de los ensayos clínicos en cortos plazos. La autorización por parte de la AEMPS suele llevar aproximadamente unos 80 días una vez todos los documentos requeridos son enviados para su evaluación, siendo España uno de los 10 países más rápidos y eficientes durante este proceso regulatorio8,9. Además, para ensayos de fase I realizados en España o terapias avanzadas para el tratamiento de enfermedades sin alternativa terapéutica las solicitudes podrán ser revisadas en 26 días tras la validación de los documentos regulatorios, permitiendo que estos ensayos puedan ser aprobados hasta en 31 días.
?
4. Investigación clínica más barata y con altos estándares: España muestra una creciente aceptación hacia los métodos de ensayo descentralizados, como la telemedicina y el monitoreo remoto. Los costos asociados con la realización de ensayos clínicos en España son competitivos en comparación con otros países. Con el auge de los ensayos descentralizados y teniendo en cuenta los costes de la investigación, España emerge como una opción muy atractiva dentro de Europa.
5. Facilitación de la innovación: La AEMPS ha creado una Oficina de Innovación para integrar, coordinar y potenciar la investigación clínica. Esta oficina ofrece asesoramiento o guía regulatoria y científica para el desarrollo de medicamentos durante cualquier etapa del ciclo de vida de este a grupos académicos, investigadores independientes, fundaciones de investigación, start-ups o fundaciones de pacientes9. Los servicios se proporcionan de forma gratuita para impulsar la innovación y permitir que la investigación académica llegue a la industria más rápidamente.
Conclusión y apuntes finales
España es uno de los líderes mundiales en ensayos clínicos. Esto se debe a que los promotores eligen España para realizar sus ensayos por la experiencia y cualificación de los investigadores, las instalaciones de primer nivel de los hospitales y la excelencia del sistema de salud, la rapidez de los procesos de autorización regulatoria, los gastos reducidos en ensayos clínicos y el potencial de reclutamiento de personas menores de edad, enfermedades raras, cáncer, trastornos mentales y enfermedades cardiovasculares y cerebrovasculares.
Todas estas características han hecho de España el país europeo con mayor crecimiento en las dos últimas décadas. Sin embargo, la aparición de nuevas tecnologías como la inteligencia artificial (IA) o el auge de la investigación clínica en países del este de Europa con menores costes asociados hacen que la inversión en este sector deba continuar aumentando para que España continue siendo referente europeo y mundial en ensayos clínicos.

| Nombre | Elisa San Isidro, Guillermo Amate y Ariadna Navarro |
|---|---|
| Empresa | Namsa |
| Cargo | Manager, Clinical Operations and Global Talent Center - Associate Clinical Study Manager - Site Director, Sr Manager Consulting, Head Global Talent Center |
Si continúas navegando, aceptas su uso.
Más información
Política de privacidad | Cookies | Aviso legal | Información adicional| miembros de CEDRO










































