Reducción del error de propagación en los análisis de muestras utilizando el sistema TFF KrosFlo® KR2i RPM?

Procesos tradicionales de filtración de flujo tangencial (TFF) se ejecutan basándose en cálculos de masa, que son propensos a errores debido a limitaciones del instrumento y al operador.
El sistema KrosFlo® KR2i RPM™ utiliza el espectrofotómetro en línea CTech™ FlowVPX® para monitorizar la concentración en tiempo real, reduciendo los riesgos asociados con los métodos tradicionales de TFF. Este artículo examina errores prácticos comunes que ocurren durante un proceso típico de ultrafiltración/diafiltración (UF/DF) e ilustra las ventajas de utilizar medición en línea de la concentración como control del proceso, en comparación con el balance de masa convencional.
Antecedentes
La filtración de flujo tangencial (TFF), es una de las técnicas de procesamiento más utilizadas en biotecnología, que separa los componentes de una solución líquida o suspensión mediante filtros de membranas. A diferencia de la filtración normal, el flujo de líquido en TFF es paralelo a la superficie de la membrana, lo que minimiza la acumulación de retenido que puede provocar el ensuciamiento de la membrana. Las moléculas más pequeñas que el tamaño del poro son forzadas a través de la membrana como resultado de una diferencia de presión; las moléculas más grandes, se recirculan al recipiente de alimentación [1]. Las aplicaciones más típicas de TFF en bioprocesamiento son la ultrafiltración (UF), por ejemplo, aumentando la concentración del producto, y diafiltración (DF), para intercambio de buffer o desalación. La filtración tangencial TFF es reconocida como una parte esencial de la mayoría de los métodos de procesamiento downstream (DSP), requiriendo así una cuidadosa consideración desde el principio del desarrollo del proceso y en el escalado de la operación [2]. Tradicionalmente, el proceso UF/DF se controla en función del cálculo de balance de masas. Aunque adoptado universalmente, este enfoque tiene considerables inconvenientes, incluido el riesgo de que se produzcan errores de cálculo, la dependencia de la pericia del operador y la necesidad de medir la concentración fuera de línea. Estos inconvenientes se mitigarían significativamente si el proceso UF/DF fuera completamente automatizado y efectivamente controlado en los parámetros críticos del proceso. La automatización de procesos implica reducción de riesgos, control estricto del proceso y eliminación del “factor humano”, entre otros beneficios [3]. El desarrollo de la automatización del proceso es complicada y exige grandes inversiones de tiempo y esfuerzo por parte del usuario final.
El sistema KrosFlo® KR2i TFF es un sistema de laboratorio ampliamente utilizado en el mercado, un sistema para TFF a escala de laboratorio, para procesos de I+D y PD en UF, DF, y con otras muchas aplicaciones. Sobre la base de este poderoso sistema, Repligen presentó recientemente el sistema RPM KrosFlo KR2i: el primer TFF del mundo que incluye el análisis de concentración en línea. No solo monitorea parámetros críticos en el proceso TFF, además permite un control activo sobre ellos aportando información en tiempo real, reduce drásticamente el coste del proceso, el tiempo y los riesgos de cometer errores. Estas características analíticas del proceso son posibles gracias a la integración del espectrofotómetro en línea FlowVPX.
Análisis en línea mediante espectroscopia de longitud de trayectoria variable
El sistema FlowVPX utiliza tecnología de longitud de trayectoria variable (VPT), un enfoque alternativo a la espectroscopia UV-Vis. VPT se basa en la ley de Beer-Lambert, donde la absorbancia es proporcional tanto a la concentración como a la longitud. Sin embargo, a diferencia de la espectroscopia UV-Vis convencional donde la longitud de la trayectoria permanece constante, VPT varía la longitud de la trayectoria para adaptarse a la concentración de la solución, lo que permite la medición de soluciones altamente concentradas sin necesidad de dilución [4].
El sistema FlowVPX basa sus mediciones en la pendiente de la absorbancia vs la longitud de trayectoria en lugar de basarse en la absorbancia absoluta, lo que permite una mayor precisión y elimina la necesidad de corrección de la línea base en la mayoría de los casos. Al integrar el instrumento FlowVPX en la ruta de flujo del sistema KrosFlo KR2i TFF (Figura 2), la concentración puede aumentarse constantemente, monitoreado y administrado en tiempo real utilizando el software dedicado KrosFlo® RPM™ (Figura 3). Todos los componentes del sistema están controlados a través de este software, que permite una automatización completa y remota de las funciones del KR2i en función de la concentración en línea mediante las mediciones del sistema FlowVPX. Además, el software RPM proporciona un análisis de datos integrado con generación de gráficos, cuadros y datos tabulares recopilados de todas las entradas y salidas que son cruciales para la comprensión del proceso, su desarrollo y optimización. El software también permite al usuario personalizar métodos, exportar informes y mantener registros de prueba detallados [5].

Los usuarios que implementen el sistema FlowVPX (como parte del sistema RPM o como instrumento independiente) deben tener en cuenta que un elemento esencial, un requisito previo para mediciones precisas, es la mezcla adecuada de la solución de alimentación. Descuidar la mezcla o mezclarla de forma inadecuada suele provocar una falta de homogeneidad en la solución, lo que empeora drásticamente las mediciones de absorbancia en línea. Al implementar FlowVPX en un laboratorio de desarrollo de procesos, se debe aplicar un agitador magnético o un reactor agitador especial a escala de laboratorio para obtener los mejores resultados.

Materiales y métodos
Para este estudio comparativo se utilizó el sistema RPM KrosFlo KR2i para realizar un proceso TFF. La concentración del producto fue monitoreada continuamente. Y simultáneamente a través del método de balance de masa convencional, usando escalas de precisión y lecturas de absorbancia en línea, usando el Sistema FlowVPX.
El sistema TFF estaba equipado con un módulo de filtro de casete HyStream 30kD SIUS PD de 0,01 m2 (EP) (artículo n.° XP030LP1E). Se utilizó el tubo de bomba de precisión L/S® L/S 14 para construir la ruta de flujo. La celda de flujo de acero inoxidable FlowVPX de 3 mm se utilizó con el Sistema FlowVPX.
El sistema TFF se utilizó en modo Concentración/Diafiltración/Concentración (C/D/C) utilizando albúmina sérica bovina (BSA). En el inicio la concentración fue de 5 mg/ml (ensayos 1 y 3) o 10 mg/ml (ensayos 2 y 4); en todas las series, la muestra se concentró a 200 mg/ml.
La presión transmembrana (TMP) se mantuvo a 0,55 bar (7,98 psi) durante las series 1, 3 y 4; la TMP fue de 1,24 bar (17,98 psi) durante la ejecución 2.
El método de medición del software RPM aplicado fue Modo Rápido a una longitud de onda de 280 nm con lectura continua, utilizando el estándar Coeficiente de extinción BSA de 0,67 (mg/ml)-1 cm-1.
Resultados y discusión
En el experimento 1, el primer objetivo de concentración (C1) fue 50 mg/ml; después, la muestra se lavó con 0,3 volúmenes de diafiltración (DV) antes del paso de concentración final (C2). En este experimento, el VPT y los métodos de balance de masa produjeron datos de concentración muy similares durante el proceso del TFF. La diferencia entre las mediciones de concentración final por cada método fue inferior al 1%.
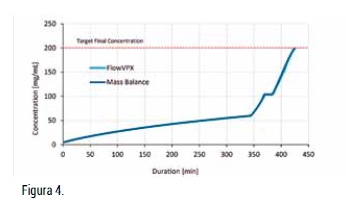
La ejecución 1 demuestra los parámetros ideales: no se produjeron interferencias no deseadas y el sistema pudo completar el proceso como corresponde a lo planificado. Las siguientes ejecuciones incluyen ejemplos de errores experimentales comunes debido, o a limitaciones inherentes del equipo o a errores humanos. Estos errores afectan el rendimiento.
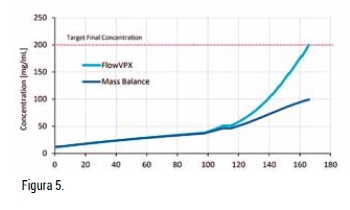
En el experimento 2, C1 fue nuevamente de 50 mg/ml, seguido de un lavado de 0,1 DV. Sin embargo, aproximadamente 100 g de líquido no fueron detectados durante el proceso del TFF. Esta magnitud de error puede ocurrir si el usuario agrega o quita accidentalmente algún peso en la báscula una vez se ha iniciado el proceso. Tal discrepancia puede surgir incluso si se ajustan los tubos del sistema, lo que afecta a la fuerza ejercida sobre el recipiente situado encima de la báscula. En este caso, el error inicial provocó una diferencia del 10% entre la concentración calculada (balance de masa) y la concentración medida (FlowVPX) al final de la fase de diafiltración, que luego creció hasta una diferencia del 50% al final de la fase de diafiltración (Figura 5).
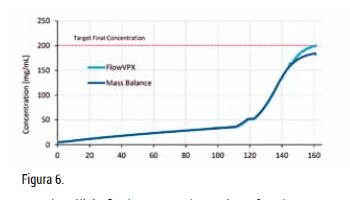
En el experimento 3, C1 fue nuevamente de 50 mg/ml, seguido de un lavado de 0,2 DV. El experimento 3 experimentó un error similar al experimento 2. Las básculas no midieron aproximadamente 7 g de líquido durante el proceso TFF, lo que resultó en una diferencia final del 9% entre el VPT, medición (200,2 mg/ml) y el cálculo del balance de masa (182,2 mg/ml) (Figura 6). Este margen de error queda fuera del rango aceptable para la mayoría de los requisitos de la industria de bioprocesamiento [6].
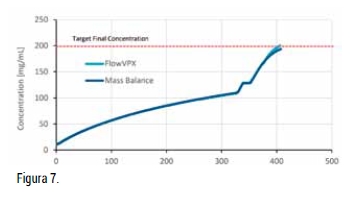
En el análisis final presentado aquí, C1 fue de 125 mg/ml, seguido de un lavado de 0,2 DV. Durante el proceso, cambios sutiles y accidentales provocaron una diferencia del 3,4% en la concentración del producto final (Figura 7). Los errores prácticos que pueden producir un error de esta magnitud pueden ser indetectables. Es poco probable que el analista detecte el error antes de que resulte en una desviación significativa del valor objetivo.
El margen del 3,4% entre la concentración medida y calculada no es tan severo como el de las series 2 y 3 y cae dentro de los límites aceptables de muchos estándares de la industria de bioprocesamiento [6]. Sin embargo, la naturaleza de este error es prácticamente imposible de rastrear hasta su origen y enfatiza el riesgo inherente al proceso cuando se emplea el método tradicional de balance de masa para determinar la concentración.
Si bien estas ejecuciones representan los resultados de varios errores conocidos y desconocidos en el proceso TFF, la característica común que comparten todos es la consistencia del sistema FlowVPX. Debido a su diseño en línea, el instrumento FlowVPX no es susceptible a esa variabilidad como lo son las escalas de precisión y, por lo tanto, logró consistentemente situarnos dentro de ±0.2% de la concentración final objetivo en todos los casos en que el método de balance de masa tuvo errores significativamente mayores.
Conclusión
El sistema RPM KrosFlo KR2i proporciona un nivel incomparable de precisión, mitigación de errores y facilidad de uso. El sistema TFF que se basa en cálculos de balance de masa exige una atención continua por parte del operador y un manejo casi perfecto del sistema y sus componentes. La integración del instrumento VPT mitiga estos problemas con una funcionalidad automatizada que logra un mayor control del proceso. El sistema permite una comprensión profunda del proceso TFF en cada paso, lo que proporciona numerosas ventajas cruciales, como son:
- Automatización independiente completa basada en un control de concentración en línea en lugar de un complicado balance de cálculo de masas.
- Reducción considerable del riesgo gracias a la gestión y el control constante en línea.
- Elimina la necesidad de realizar mediciones fuera de línea que consumen mucho tiempo, lo que proporciona información solo después de que el proceso ya ha finalizado.
- Integración total del software, combinando las funciones innovadoras del sistema FlowVPX con la versatilidad del KrosFlo KR2i.
- Alta capacidad de personalización debido al diseño modular y la disponibilidad de componentes listos parausar, como rutas de flujo, sensores y contenedores (también disponibles como artículos de un solo uso).
Estos beneficios hacen del sistema RPM KrosFlo KR2i una excelente opción para los usuarios nuevos y existentes de FlowVPX y KR2i que buscan aumentar la eficiencia y reducir el riesgo en sus operaciones de investigación y desarrollo TFF.
Bibliografía
- van Reis R, Zydney A. Membrane separations in biotechnology. Current Opinions in Biotechnology. 2001 Apr; 12(2):208-11.
- Straathof AJJ, Wahl SA, Benjamin KR, Takors R, Wierckx N, Noorman HJ. Grand Research Challenges for Sustainable Industrial Biotechnology. Trends in Biotechnology. 2019 Oct; 37(10):1042-1050.
- Holstein, M, Hung, J, Feroz, H, et al. Strategies for high-concentration drug substance manufacturing to facilitate subcutaneous administration: A review. Biotechnology and Bioengineering. 2020; 117: 3591–3606.
- Huffman, S.; Soni, K.; Ferraiolo, J. UV-Vis Based Determination of Protein Concentration: Validating and Implementing Slope Measurements Using Variable Pathlength Technology. Bioprocess International. 2014; 12(8): 2–8. https://bioprocessintl.com/manufacturing/monoclonal-antibodies/uv-vis-based-determination-protein-concentrationvalidating-implementing-slope-measurements-using-variable-pathlength-technology/.
- DOC0302 - KrosFlo® KR2i RPM™ System - Product Specifications Sheet. Published: Feb 14 2023. eRev. 01. https://www.repligen.com/ctechresources/pdf/DOC0302%20KrosFlo%20KR2i%20RPM%20System%20Specification%20Sheet.pdf.
- Thomas A. Little. Establishing Acceptance Criteria for Analytical Method. BioPharm International-10-01-2016, Volume 29, Issue 10 https://www.biopharminternational.com/view/establishing-acceptance-criteria-analytical-methods
| Nombre | Oleksandr Karpenko, Westley Blacklock, Jigar Patel, Brandon Goldberg, Joe Ferraiolo, Blas Pinar |
|---|---|
| Empresa | Repligen |
| Cargo |
Si continúas navegando, aceptas su uso.
Más información
Política de privacidad | Cookies | Aviso legal | Información adicional| miembros de CEDRO









































