Las terapias con células T modificadas genéticamente representan un hito revolucionario en el tratamiento de distintos tipos de cáncer como la leucemia linfoblástica aguda, ciertos linfomas y el mieloma múltiple.
En todos ellos, las células inmunológicas del propio paciente se modifican con receptores de antígenos quiméricos (CAR); y una vez reintroducidas en el paciente, instruyen al sistema inmunológico para reconocer y eliminar las células tumorales.
La generación de células CAR-T implica cinco pasos básicos. En primer lugar, las células T se aíslan del plasma sanguíneo del paciente. Posteriormente, las células se activan para aceptar un vector viral que contiene la construcción genética para el CAR. Después se expanden en cultivo y, finalmente, se administran al paciente por vía intravenosa. Aunque las terapias aprobadas usan muestras de pacientes, hay interés en utilizar células T alogénicas proporcionadas por donantes1.
Dado que las terapias con células CAR-T provienen del donante, cada dosis fabricada es única; lo que origina importantes desafíos en cuanto al control de calidad se refiere, pues debe garantizarse que, tras la fabricación, almacenamiento, envío y administración, la dosis final cumple con los criterios de seguridad, estabilidad y potencia necesarios2.
Una herramienta importante que ayuda a verificar la identidad celular a lo largo del proceso de fabricación es el análisis de las repeticiones cortas en tándem (del inglés Small Tandem Repeats), una técnica de identificación genética ampliamente utilizada en la comunidad forense y que también se emplea como método de elección para autenticar líneas celulares en investigación3.
El genoma humano contiene regiones de ADN repetitivo, denominadas regiones hipervariables, que consisten en una secuencia corta de ADN repetida en tándem. Estas regiones STR son polimórficas, ya que la secuencia varía en el número de copias de la unidad repetida. Las longitudes de cualquier alelo STR dado variarán de un individuo a otro, y medir por electroforesis capilar la longitud de múltiples alelos STR proporciona perfiles genéticos fiables.
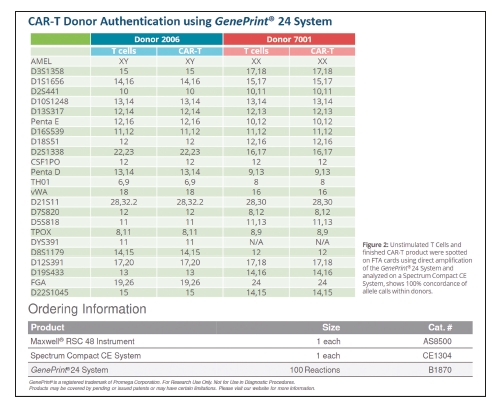
En la fabricación de células CAR-T, el perfil STR se puede recopilar en cualquier momento del proceso para confirmar que las células derivan del paciente o donante original. En primer lugar, se recopila un perfil STR de referencia a partir de un subconjunto de células aisladas del paciente. Luego, las células se analizan en diversas etapas durante el proceso de fabricación para confirmar que el perfil resultante coincida con el original. Si se producen confusiones de muestras o si las muestras se contaminan con células de otros individuos en la fabricación, almacenamiento o envío, el análisis STR lo identifica.
El análisis STR también puede emplearse en terapias experimentales sobre el uso de células T alogénicas, y así emplear células recolectadas en donantes sanos, determinando el porcentaje de células CAR-T alogénicas en una mezcla de células y sabiendo los niveles relativos de células del paciente y del donante presentes en una muestra.
Además, permite hacer el seguimiento postrasplante y analizar los posibles quimerismos que puedan surgir en el caso de que las células cancerígenas del huésped vuelven a proliferar.
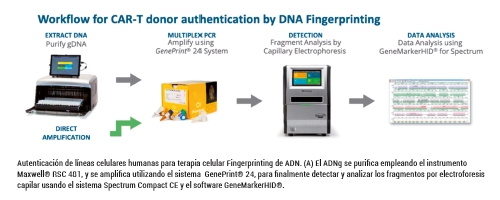
Promega ofrece instrumentación y reactivos que cubren la totalidad del flujo de trabajo, desde la extracción de la muestra hasta su análisis por electroforesis capilar.
Otras terapias celulares
Promega también ofrece tecnología luminiscente para optimizar y desarrollar terapias celulares personales y efectivas en las que son necesarias mediciones cuantitativas en tiempo real y entornos celulares vivos.
Este es el caso de abordajes terapéuticos basados en la degradación dirigida de proteínas como la Casein kinasa 1α, (CK1α), relacionada con la proliferación celular descontrolada e implicada en diversos procesos patológicos como el mieloma múltiple y cáncer de tipo hematológico4. En este estudio, los autores emplean CellTiter-Glo y NanoBRET, tecnología luminiscente de Promega, para cribar seleccionar y perfilar la molécula SJ7095 con potencial utilidad como degradador selectivo de CK1α y posible anticancerígeno de amplio espectro.
Referencias
- Depil, S. et al. (2020) ‘Off-the-shelf’ allogeneic CAR T cells: development and challenges. Nat. Rev. Drug Discov. 19, 185–199.
- U.S. Department of Health and Human Services, Food and Drug Administration (2020) Chemistry, Manufacturing, and Control (CMC) Information for Human Gene Therapy Investigational New Drug Applications (INDs): Guidance for Industry.
- ATCC SDO (2021) Human Cell Line Authentication: Standardization of Short Tandem Repeat (STR) Profiling. ATCC Standards Development Organization, Manassas, VA
- Nishiguchi, G., Mascibroda, L.G., Young, S.M. et al. Selective CK1α degraders exert antiproliferative activity against a broad range of human cancer cell lines. Nat Commun 15, 482 (2024). https://doi.org/10.1038/s41467-024-44698-1
Descarga sugerida:
Artículo escrito por:
Promega Biotech Ibérica SL




