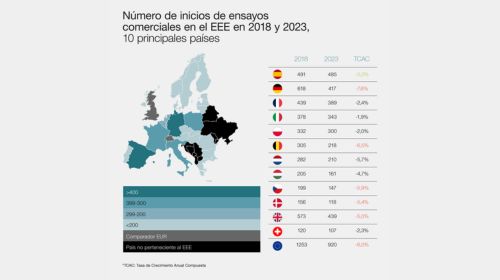
En 2023, España superó a Alemania como el país que más ensayos clínicos inició, consolidándose como el líder europeo en este ámbito. Así lo refleja el informe "Evaluando el ecosistema de ensayos clínicos en Europa," elaborado por la consultora Iqvia para Efpia y Vaccines Europe. Aunque destaca el papel de España, el informe advierte sobre la pérdida de competitividad de Europa frente a Estados Unidos y China.
Entre 2013 y 2023, el número de pacientes reclutados para ensayos clínicos impulsados por la industria en todo el mundo ha aumentado un 12%, mientras que el porcentaje de pacientes europeos ha disminuido un 20%. Esto significa que 60,000 pacientes europeos han perdido la oportunidad de acceder a nuevos medicamentos en fase experimental entre 2018 y 2023.
Desafíos para Europa
Aunque el número total de ensayos clínicos ha aumentado un 38% en este período, el porcentaje de ensayos realizados en Europa ha caído del 22% al 12%. La situación es similar en todos los países del Espacio Económico Europeo (EEE), a excepción de Portugal, Eslovaquia y Grecia; España ha mantenido una ligera disminución del 0.2%. El informe señala problemas sistémicos comunes en el ecosistema de investigación en Europa, destacando que los ensayos clínicos europeos enfrentan un entorno de investigación lento y fragmentado.
Nathalie Moll, directora general de Efpia, enfatiza que “para que Europa sea competitiva, debe funcionar como una región unificada y no como Estados Miembros individuales,” respaldada por políticas que atraigan inversiones. Solo así los europeos podrán disfrutar de las mismas oportunidades de acceso a avances médicos que en otras partes del mundo.
Incremento en ensayos clínicos en China
Durante el mismo período en que Europa pierde competitividad, China ha incrementado su participación en ensayos clínicos, pasando del 5% al 18% del total. Mientras tanto, Estados Unidos ha disminuido del 28% al 23%, y Asia (sin contar a China y Japón) ha aumentado del 11% al 15%.
El informe también muestra caídas en áreas clave como oncología, inmunización, enfermedades raras, y terapias celulares y génicas, donde la cuota europea ha descendido del 25% al 10%. En contraste, China ha incrementado su cuota del 10% al 42%, gracias a un entorno regulatorio favorable y un enfoque estratégico hacia las terapias avanzadas. Además, el informe advierte sobre el declive en ensayos pediátricos y en ensayos de fase 1, cruciales para el desarrollo clínico posterior.
España: un caso de éxito en ensayos clínicos
En este contexto de pérdida de competitividad, el informe resalta a España como un caso de éxito, logrando la primera posición por el número de ensayos iniciados en 2023. Este éxito se atribuye principalmente a la implementación de la regulación de ensayos clínicos (CTR) europea, que España fue la primera en adoptar en 2016. La inversión en ensayos clínicos ha crecido a un ritmo del 5.7% anual, pasando de 479 millones en 2012 a 834 millones en 2022.
Entre los factores que han contribuido a atraer inversiones, el informe menciona:
- La calidad del sistema de salud español, incluida la infraestructura hospitalaria.
- La exitosa implementación de la nueva legislación europea sobre ensayos clínicos y la adaptación de la legislación nacional.
- Un modelo de colaboración efectivo entre ensayos clínicos promovidos por la industria y los públicos.
- La ubicación de centros de investigación clave en varias ciudades, con más de tres centros de investigación por cada 10,000 km² en el país.
- En inmunización, se inician aproximadamente 20 ensayos al año en España, excluyendo los años de la pandemia de COVID-19.
Estrategias para consolidar el liderazgo
A pesar de su posición como líder en ensayos clínicos, la industria farmacéutica innovadora en España enfrenta desafíos para consolidar su liderazgo y recuperar la competitividad europea. Entre las estrategias propuestas se incluyen:
- La agilización y reducción de procesos de gestión en investigación clínica, incluyendo la implementación de un proceso de fast track para ensayos de fase 1 y la simplificación de la burocracia.
- El fomento de la investigación clínica en Atención Primaria con una guía de recomendaciones propuesta por Farmaindustria.
- La promoción de ensayos clínicos descentralizados y en red, el uso de datos en vida real, y la difusión de una guía de excelencia para realizar ensayos clínicos en Farmacia Hospitalaria.
Amelia Martín Uranga, directora de Investigación Clínica y Traslacional de Farmaindustria, subraya que “los desafíos para mantener la competitividad y reforzar el liderazgo en España son cada vez mayores.”
Necesidad de reformas urgentes
Los ensayos clínicos ofrecen beneficios significativos, especialmente en enfermedades raras, al acelerar la llegada de fármacos al paciente. Además, generan beneficios económicos y para el sistema sanitario, como el aumento del empleo y capacidades del sistema. El informe estima que los beneficios para los sistemas de salud de la UE por ensayos clínicos y ahorros en medicamentos oscilan entre 1,000 y 1,500 millones de euros.
Por todo esto, los autores del informe instan a abordar la pérdida de competitividad con urgencia. Se requiere la implicación de todas las partes involucradas y la implementación de políticas públicas que reconozcan la importancia de los incentivos regulatorios a la innovación. Esto incluye una evaluación urgente del Reglamento de Ensayos Clínicos y medidas para armonizar y simplificar el panorama de ensayos clínicos en toda la UE, facilitando así ensayos clínicos multinacionales. Además, se aboga por ampliar la capacidad para ensayos y mejorar las infraestructuras, emulando el desempeño de España.