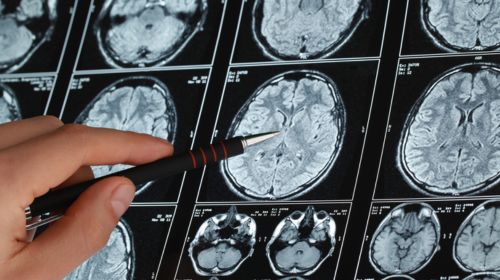
Un estudio pionero descubre que los tumores cerebrales ‘hackean’ la comunicación entre las neuronas

En el trabajo han colaborado los laboratorios de Manuel Valiente (CNIO) y Liset Menéndez de La Prida (Instituto Cajal del CSIC).
Casi la mitad de los pacientes con metástasis cerebral ven afectada su capacidad cognitiva. Hasta ahora se asumía que esto se debe a la presencia física del tumor, que presiona el tejido neuronal. Pero algo falla en esa hipótesis del efecto masa del tumor, porque a menudo no hay relación entre el tamaño del cáncer y su impacto cognitivo. Tumores pequeños pueden generar alteraciones importantes, y a la inversa. ¿Por qué? La explicación puede estar en que la metástasis cerebral hackea la actividad del cerebro, según demuestra por primera vez un estudio publicado en Cancer Cell al que la revista ha otorgado su portada en la edición impresa.
Los autores, del Consejo Superior de Investigaciones Científicas (CSIC) y el Centro Nacional de Investigaciones Oncológicas (CNIO), han descubierto que cuando el cáncer se disemina en el cerebro (hace metástasis) altera la química cerebral, e interfiere así en la comunicación neuronal -las neuronas se comunican mediante impulsos eléctricos que se generan y transmiten mediante cambios bioquímicos en las células y su entorno-.
En el trabajo han colaborado los laboratorios de Manuel Valiente (CNIO) y Liset Menéndez de La Prida (Instituto Cajal del CSIC) dentro del proyecto europeo NanoBright, destinado a desarrollar nuevas tecnologías para el estudio del cerebro, y con participación de otras agencias financiadoras como MICINN, AECC, ERC, NIH y EMBO.
Demostración con inteligencia artificial
Los investigadores midieron la actividad eléctrica del cerebro de ratones con y sin metástasis, y observaron que los registros electrofisiológicos de los animales con cáncer son distintos. Para asegurarse de que esa diferencia es atribuible a la metástasis recurrieron a la inteligencia artificial. Entrenaron a un sistema de inteligencia artificial con numerosos registros electrofisiológicos y, en efecto, el modelo aprendió a identificar la presencia de metástasis.
Estos resultados muestran que, la metástasis influye en la actividad eléctrica cerebral de manera específica, dejando una huella muy clara.
El estudio supone, para los autores, un “cambio de paradigma” en el conocimiento básico sobre cómo se desarrolla la metástasis cerebral, y tiene implicaciones para la prevención, el diagnóstico precoz y el tratamiento de esta patología.
En la pista de un fármaco contra los efectos neurocognitivos
Además de registrar los cambios en la actividad eléctrica cerebral en presencia de metástasis, los investigadores han empezado a explorar los cambios bioquímicos que explicarían esta alteración. Analizando los genes que se están expresando en los tejidos afectados han identificado una molécula, EGR1, con un papel potencialmente importante en el proceso. El hallazgo abre la posibilidad de diseñar un fármaco que prevenga o palíe los efectos neurocognitivos de la metástasis cerebral.
Como explica Valiente, director del grupo de Metástasis Cerebral del CNIO, “nuestro estudio multidisciplinar cuestiona el hecho hasta ahora aceptado de que la disfunción neurológica, muy habitual en pacientes con metástasis cerebral, se debe únicamente al efecto masa del tumor. Nosotros proponemos que estos síntomas son consecuencia de cambios en la actividad cerebral producto de las alteraciones bioquímicas y moleculares, inducidas por el tumor. Es un cambio de paradigma que podría tener implicaciones relevantes para el diagnóstico y las estrategias terapéuticas”.
Liset Menéndez de La Prida, directora del Laboratorio de Circuitos Neuronales del Instituto Cajal (CSIC), señala: “Mediante aprendizaje automático hemos sido capaces de integrar todos los datos para crear un modelo que permite saber si hay o no metástasis cerebral mirando únicamente a la actividad eléctrica. Esta aproximación computacional podría tener la capacidad incluso de predecir subtipos de metástasis cerebral en estadios iniciales. Es un trabajo totalmente pionero, que abre un camino inexplorado”.
Ambos autores resaltan el carácter multidisciplinar de un trabajo complejo que combina neurociencia, investigación oncológica y computacional, y cada una de estas áreas con, a su vez, un amplio abanico de técnicas diferentes.
Estudio cognitivo de pacientes y desarrollo de técnicas no invasivas
El cambio de enfoque que aporta este resultado hace que los investigadores quieran analizar mucho más sistemáticamente el estado cognitivo de los pacientes con metástasis cerebral. Este es, para Valiente, uno de los principales próximos pasos. Para ello será clave RENACER, la Red Nacional de Metástasis Cerebral promovida por el CNIO, que ya ha servido para generar la mayor colección de muestras vivas de metástasis cerebral en el mundo (con el consentimiento de los pacientes, las muestras extraídas en quirófano quedan a disposición de la comunidad científica internacional en el Biobanco CNIO), y en la que ahora van a introducir protocolos de evaluación neurocognitiva de los pacientes participantes.
Menéndez de La Prida, por su parte, avanzará en la integración del registro de la actividad cerebral con el análisis de las moléculas implicadas, “para desarrollar nuevas sondas diagnósticas de tumores cerebrales”, señala. Es una tarea en línea con el proyecto europeo NanoBright, que busca crear técnicas no invasivas para investigar el cerebro y tratar sus patologías, y en el que participan el CSIC y el CNIO.
Otro objetivo es dar con fármacos que protejan al cerebro de las interferencias creadas por el cáncer en los circuitos neuronales utilizando las novedosas estrategias ya mencionadas. “Buscaremos las moléculas que juegan un papel en las alteraciones inducidas por la metástasis en la comunicación neuronal, y las evaluaremos como posibles dianas terapéuticas”, explica Valiente. Además de la inteligencia artificial ideada por el equipo del CSIC, emplearán la tecnología METPlatform desarrollada en el CNIO para evaluar la posible actividad terapéutica de cientos de compuestos a la vez sobre las muestras de tejido cerebral afectadas por la metástasis.
Y ADEMÁS



Si continúas navegando, aceptas su uso.
Más información
Política de privacidad | Cookies | Aviso legal | Información adicional| miembros de CEDRO